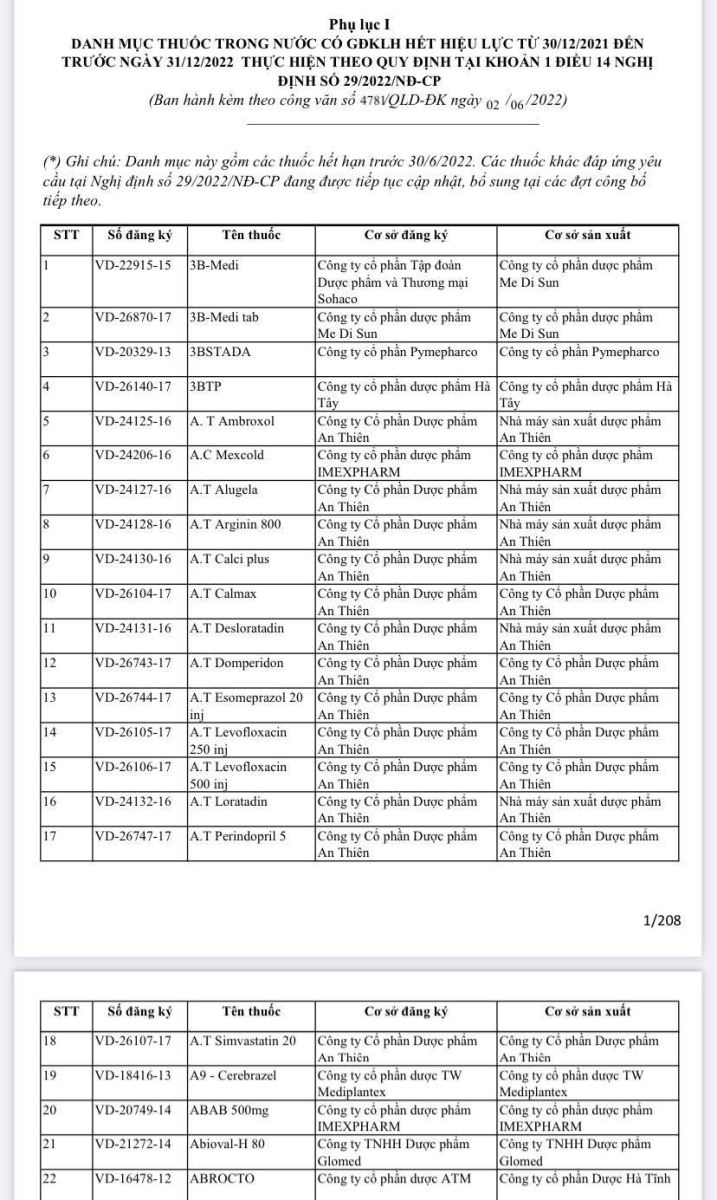
 Danh mục một số thuốc trong nước có giấy đăng ký lưu hành hết hạn từ 31/12/2021 đến trước 31/12/2022.
Danh mục một số thuốc trong nước có giấy đăng ký lưu hành hết hạn từ 31/12/2021 đến trước 31/12/2022.
Trước đó, theo Nghị định 29/2022/NĐ-CP của Chính phủ ngày 29/4/2022 quy định chi tiết và biện pháp thi hành Nghị quyết số 12/2021/UBTVQH15 của Uỷ ban thường vụ Quốc hội về việc cho phép thực hiện một số cơ chế, chính sách trong lĩnh vực y tế để phục vụ công tác phòng, chống dịch COVID-19, Bộ Y tế có trách nhiệm công bố trên Cổng thông tin điện tử của Bộ danh mục các thuốc, nguyên liệu làm thuốc có giấy đăng ký lưu hành hết hiệu lực trong khoảng thời gian từ ngày Nghị quyết số 12/2021/UBTVQH15 có hiệu lực đến trước ngày 31/12/2022 nhưng do ảnh hưởng của đại dịch COVID-19 nên chưa thể hoàn thành thủ tục gia hạn đăng ký lưu hành thì được tiếp tục sử dụng đến hết ngày 31/12/2022.
Trong số danh mục 6.251 thuốc vừa được Cục Quản lý Dược công bố gia hạn sử dụng, có 4.631 thuốc sản xuất trong nước; 1.427 thuốc nước ngoài và 193 vaccine, sinh phẩm. Danh mục này chỉ gồm các thuốc có đăng ký lưu hành hết hạn trước ngày 30/6/2022.
Các thuốc khác đáp ứng yêu cầu tại Nghị định số 29/2022/NĐ-CP hết hạn đăng ký lưu hành trong khoảng từ ngày 1/7-31/12/2022, Cục Quản lý Dược đang tiếp tục cập nhật, bổ sung trong các đợt công bố sau đó.
Thông tin chi tiết của từng thuốc tra cứu theo số đăng ký công bố trong danh mục tại địa chỉ https://dichvucong.dav.gov.vn/congbothuoc/index.
Riêng với các thuốc, nguyên liệu làm thuốc trong danh mục đã thực hiện thay đổi, bổ sung trong quá trình lưu hành hoặc có đính chính thông tin liên quan đến giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc, doanh nghiệp xuất trình văn bản phê duyệt hoặc xác nhận của Bộ Y tế (Cục Quản lý Dược) với các cơ quan, đơn vị liên quan để thực hiện các thủ tục theo quy định pháp luật.
Theo Thứ trưởng Bộ Y tế Đỗ Xuân Tuyên, danh mục các thuốc này sẽ tự động được gia hạn, các doanh nghiệp không phải thực hiện thêm bất kỳ thủ tục gì.
Việc công bố danh mục thuốc này đồng nghĩa với việc sẽ có thêm nhiều thuốc được lưu hành trên thị trường Việt Nam, tránh tình trạng khan hiếm hoặc hết thuốc chữa bệnh ở một số cơ sở y tế.