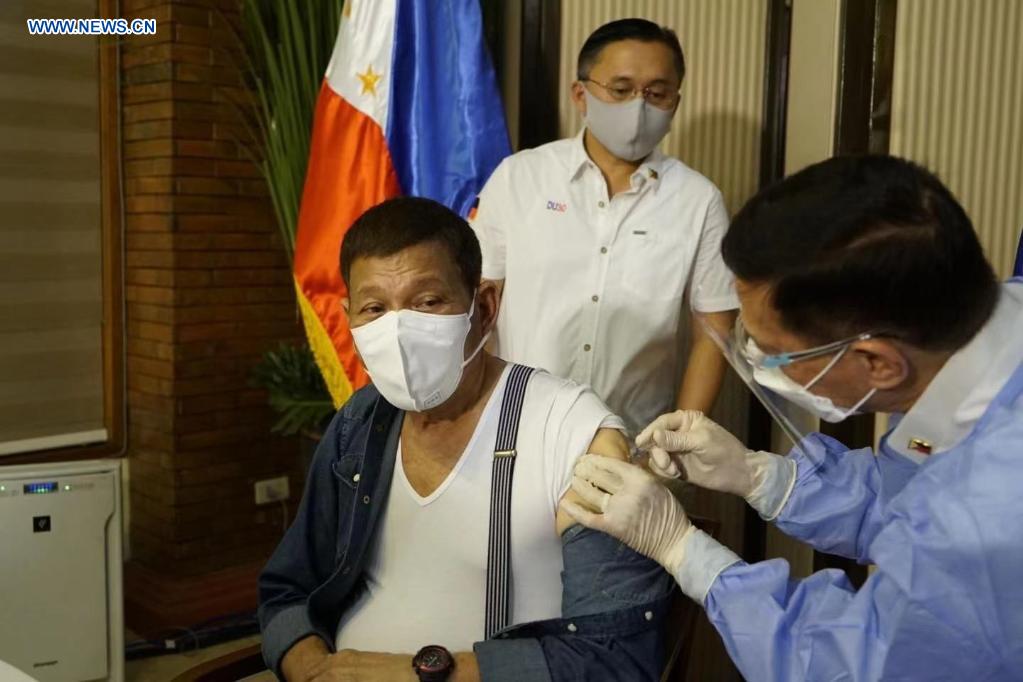
 Tổng thống Philippine Rodrigo Duterte (trái) tiêm vaccine phòng COVID-19 của Sinopharm/Trung Quốc ngày 3/5/2021. Ảnh: Xinhua
Tổng thống Philippine Rodrigo Duterte (trái) tiêm vaccine phòng COVID-19 của Sinopharm/Trung Quốc ngày 3/5/2021. Ảnh: Xinhua
Theo CNN, ông Rodrigo Duterte ngày 4/5 đã đề nghị Trung Quốc nhận lại khoản viện trợ 1.000 liều vaccine do công ty Sinopharm sản xuất với lý do công ty này chưa nộp đơn xin cấp phép chính thức lên Cơ quan Quản lý Thực phẩm và Dược phẩm (FDA) Philippines.
Ông Duterte cũng xin lỗi vì đã tiêm phòng COVID-19 bằng vaccine của Sinopharm trong khi vaccine này chưa được cấp phép sử dụng tại Philippines.
Trước đó, nhà lãnh đạo Philippines đã bị dư luận trong nước chỉ trích vì tiêm phòng vaccine Sinopharm dù vaccine của Trung Quốc chưa được FDA Philippines phê duyệt.
Ông Duterte thừa nhận đã tiêm mũi vaccine Sinopharm đầu tiên vào ngày 3/5, nhưng lưu ý rằng tốt hơn là nên tránh các vấn đề bằng cách thu hồi loại vaccine này. “Các bạn đúng, chúng tôi sai. [Vaccine] Sinopharm sẽ bị loại bỏ vào ngày mai hoặc ngày kia. Tôi đã thực hiện điều đó như một yêu cầu cá nhân”, ông Duterte nói.
Tuy nhiên, ông khẳng định rằng việc sử dụng Sinopharm của mình là "hợp pháp". “Khi chính phủ cho phép vaccine đó được sử dụng cho mục đích nhân đạo, bản thân đó đã là một thẩm quyền để mọi người được tiêm”, Tổng thống Philippines nói.
Mặc dù vậy, do vaccine Sinopharm chưa được FDA Philippines phê duyệt, ông Duterte khuyến cáo công chúng không nên tiêm vaccine này.
Bên cạnh việc yêu cầu Đại sứ Trung Quốc rút lại lô vaccine Sinopharm, nhà lãnh đạo Philippines đề nghị đại diện Bắc Kinh cung cấp vaccine phòng COVID-19 từ một nhà sản xuất khác là Sinovac Biotech. Philippines vốn đã nhận 3,5 triệu liều vaccine CoronaVac của hãng Sinovac, trong đó có 1 triệu liều do chính phủ Trung Quốc tài trợ.
 Xi-lanh chứa vaccine phòng COVID-19 của công ty Sinopharm, Trung Quốc. Ảnh: Reuters
Xi-lanh chứa vaccine phòng COVID-19 của công ty Sinopharm, Trung Quốc. Ảnh: Reuters
Vaccine phòng COVID-19 của Sinopharm, với 2 mũi tiêm, đạt hiệu quả chung là 78,1% bảo vệ bệnh nhân khỏi lây nhiễm COVID-19 – theo số liệu mà Sinopharm cung cấp cho Tổ chức Y tế Thế giới (WHO).
Tuy nhiên theo Reuters, các chuyên gia của WHO cho rằng "rất ít tin tưởng" vào một số dữ liệu mà Sinopharm cung cấp về vaccine COVID-19 của họ, liên quan đến nguy cơ mắc các tác dụng phụ nghiêm trọng ở một số bệnh nhân. Tuy vậy, nhìn chung chuyên gia WHO vẫn tin tưởng vào khả năng ngăn ngừa bệnh của loại vaccine này.
Một người phát ngôn của WHO cho biết tài liệu về vaccine BBIBP-CorV của Sinopharm là "một trong nhiều nguồn" để đưa ra các khuyến nghị, dự kiến sẽ được WHO ban hành vào cuối tuần này.
Tài liệu "đánh giá bằng chứng" nói trên do Nhóm chuyên gia cố vấn chiến lược của WHO (SAGE) chuẩn bị nhằm đánh giá về vaccine phòng COVID-19 của Sinopharm, vốn đã được 45 quốc gia và khu vực pháp lý cho phép sử dụng ở người lớn, với 65 triệu liều đã được tiêm.
Tài liệu bao gồm tóm tắt dữ liệu từ các thử nghiệm lâm sàng ở Trung Quốc, Bahrain, Ai Cập, Jordan và Các Tiểu vương quốc Ả Rập Thống nhất.
Tài liệu của WHO cho biết, hiệu quả của vaccine Sinopharm trong các thử nghiệm lâm sàng ở giai đoạn 3 ở nhiều quốc gia là 78,1% sau hai liều. Con số này giảm nhẹ so với mức 79,34% được công bố trước đó ở Trung Quốc.
Phân tích SAGE với vaccine phòng COVID-19 của Sinopharm được chuẩn bị khi một nhóm cố vấn kỹ thuật của WHO hiện đang xem xét vaccine này để phê duyệt sử dụng khẩn cấp. Điều này không chỉ mở đường cho việc sử dụng vaccine Sinopharm trong nền tảng chia sẻ vaccine COVAX toàn cầu mà còn cung cấp sự chứng thực quốc tế quan trọng cho vaccine được phát triển bởi Trung Quốc.