AstraZeneca ngày 22/3 đã đưa ra thông báo trên, mở đường để công ty này chính thức xin cấp phép lưu hành vaccine của hãng tại Mỹ.
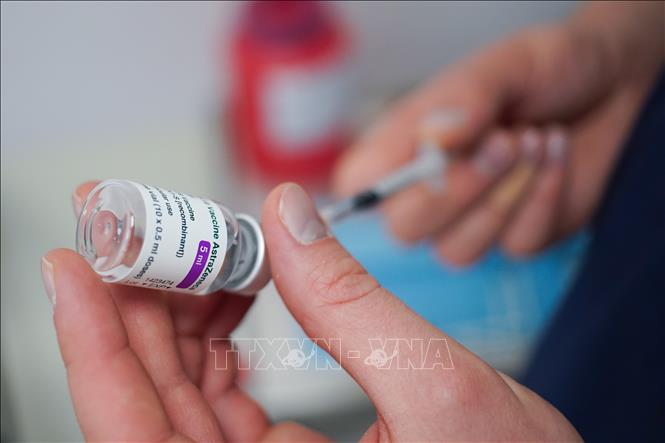 Vaccine ngừa COVID-19 của hãng dược AstraZeneca. Ảnh: PAP/TTXVN
Vaccine ngừa COVID-19 của hãng dược AstraZeneca. Ảnh: PAP/TTXVN
Theo AstraZeneca, trong giai đoạn thử nghiệm sau cùng được tiến hành với sự tham gia của 32.000 người tình nguyện ở mọi lứa tuổi, vaccine của hãng đạt hiệu quả 100% phòng chống triệu chứng nghiêm trọng của bệnh COVID-19 và ngăn ngừa nguy cơ phải nhập viện điều trị, và đảm bảo an toàn.
AstraZeneca cho biết thêm một ủy ban an toàn độc lập cũng đã tiến hành đánh giá cụ thể về các trường hợp xuất hiện cục đông máu trong các cuộc thử nghiệm tại Mỹ cũng như tình trạng xuất hiện huyết khối tĩnh mạch não (CVST) với sự trợ giúp của một chuyên gia về thần kinh độc lập.
Ủy ban này cũng đã đưa ra kết luận không có nguy cơ gia tăng hiện tượng huyết khối hoặc các biến chứng liên quan đến huyết khối trong số 21.583 người được tiêm chủng ít nhất 1 mũi vaccine. Cũng không xuất hiện tình trạng xuất hiện huyết khối tĩnh mạch não ở bất cứ trường hợp nào trong cuộc thử nghiệm này.
Căn cứ vào kết quả thử nghiệm trên, Giáo sư Sarah Gilbert thuộc Đại học Oxford cho biết AstraZeneca và Đại học Oxford sẽ chuẩn bị dữ liệu để xin cấp phép lưu hành vaccine của Cơ quan quản lý dược phẩm và thực phẩm (FDA), Mỹ.